qPCR:从样品采集到表达量计算
参考文献
采样计划
- 有多少个处理?
- 每个处理有几个生物学重复?
- 每个生物学重复做几次技术重复?
- 要检测多少个目标基因(包括内参基因)?
采样之前规划好,准备好相应的离心管等耗材。

如何采样
采样时间选择
采样时间会影响基因的表达,很可能在采样时间点目标基因没有发生转录表达,也就是刚好碰上转录表达的窗口期。最好是有预实验确定采样时间点。

采样部位选择
那么多组织部位,如何选择呢?混采的结果很可能是没有差异,最好是具有组织部位特异性(下图)。比如水稻叶片,通常采旗叶🚩的中间部位。
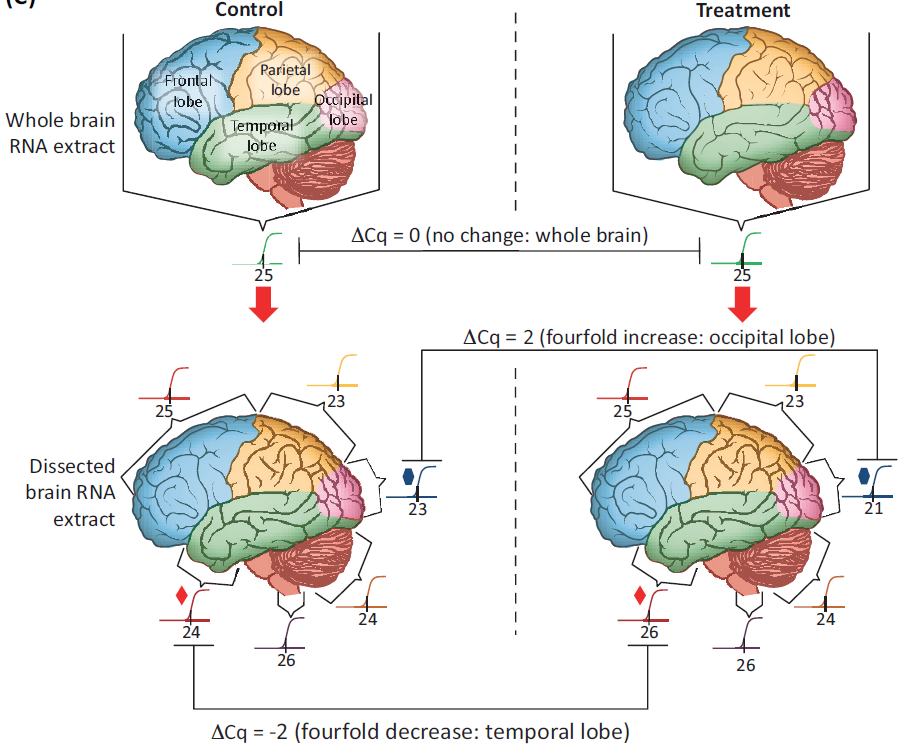
我的采样Tips:
每个样品至少分装成2管子;
- 一管用于qPCR,另外一管用于其他组学;
- 第一次提取RNA失败的时候还有机会再提一次。
不同的生物学重复混为一个样品,减少生物学重复中间的差异。比如我有4个生物学重复,那我就从4个生物学重复中各选一株的旗叶,混为第一个生物学重复的样品,分装为2管。
如何点样
点样分为两个部分:
- Mix:除开cDNA以外的所有成分,包括引物、qPCR Mix和H$_2$O.
- cDNA:从RNA反转录来的cDNA.
需要如下的阴性对照:
- H$_2$O:检测使用的H$_2$O是否有污染(最好是将大瓶的RNA-free Water分装到小的离心管中,一次一管,用完就丢,避免影响后续的试验);
- RNA样品:检测是否有基因组DNA污染。

技术重复
当cDNA的浓度很低时,在第一个循环时,加入的引物不能结合到所有的靶标片段,会导致最后扩增的结果差异较大,出现这种情况的书哈就需要将不同的生物学重复的结果取平均值用于后续计算。
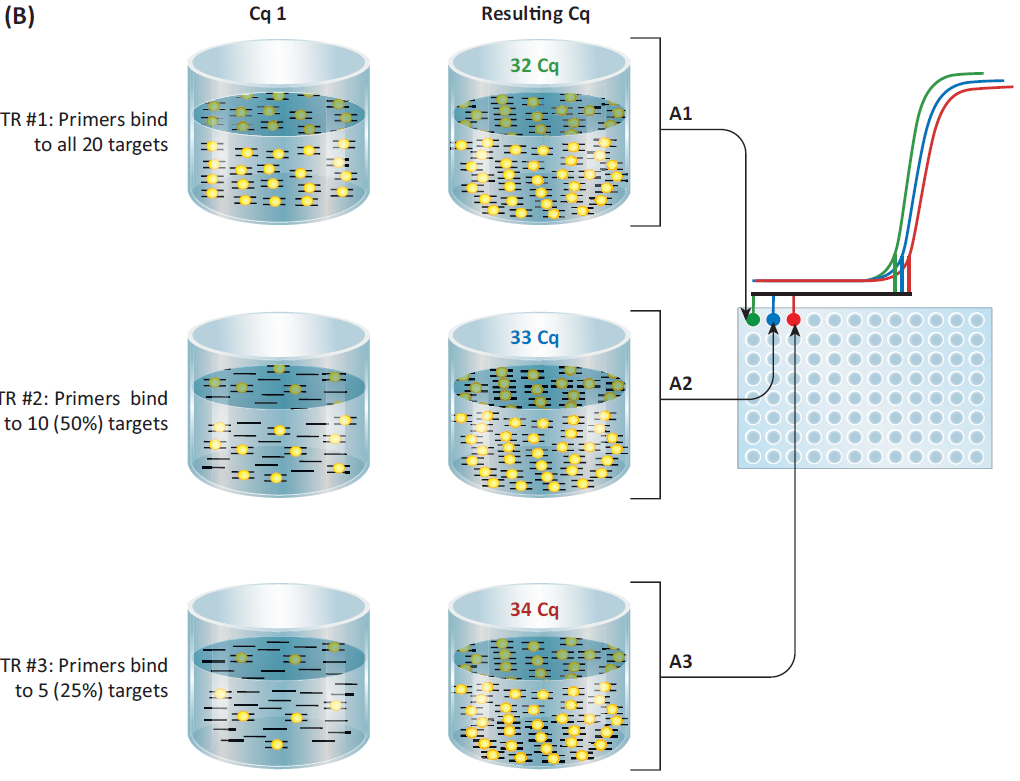
关于引物
引物要求一:溶解曲线是单峰
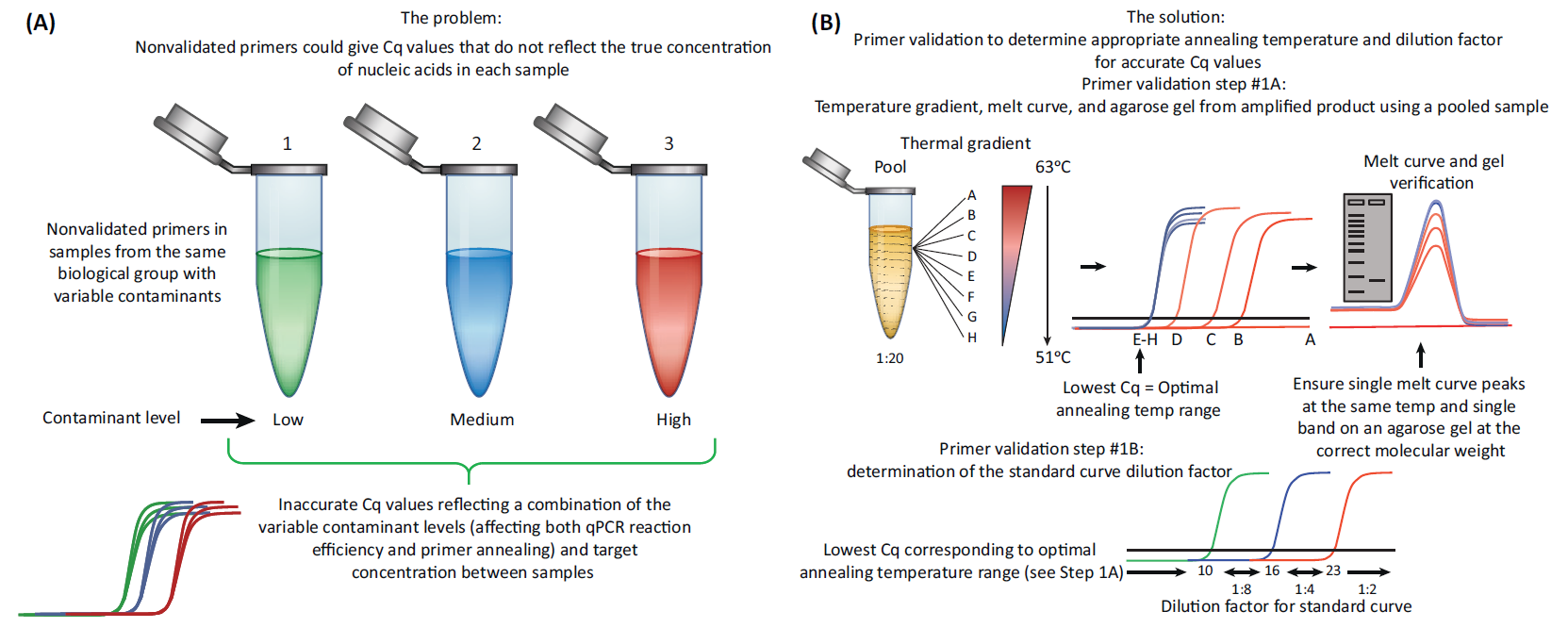
引物要求二:扩增效率范围
采样梯度稀释的方法计算引物的扩增效率。如何从稀释倍数计算引物的扩增效率(参考帖子)?相关工具参考qPCRtools.
另外一个重要的点是内参基因,内参基因不稳定会导致结果差异很大。
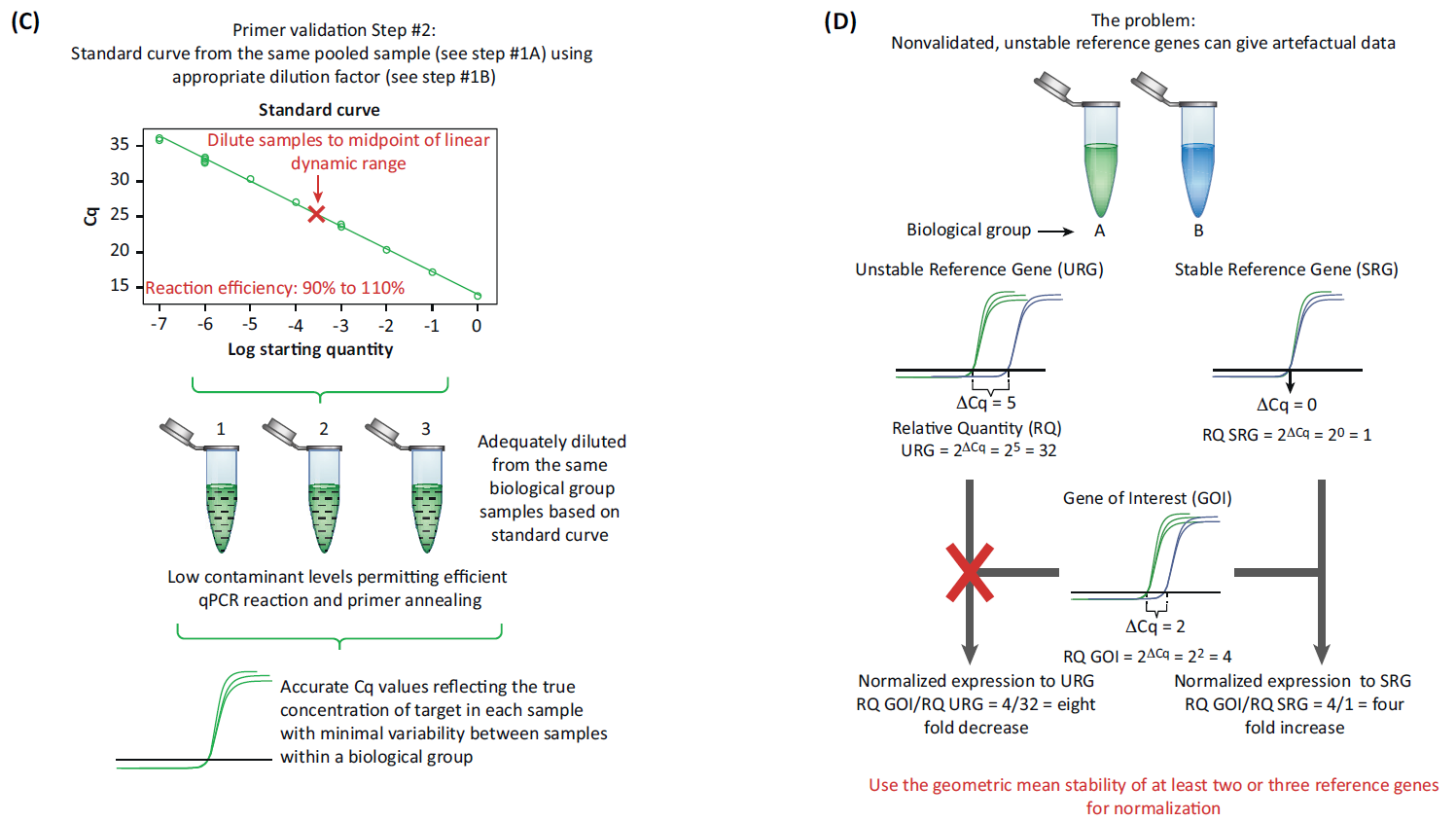
表达量计算
最常见的方法是2$^{-{\delta}{\delta}C_t}$法:
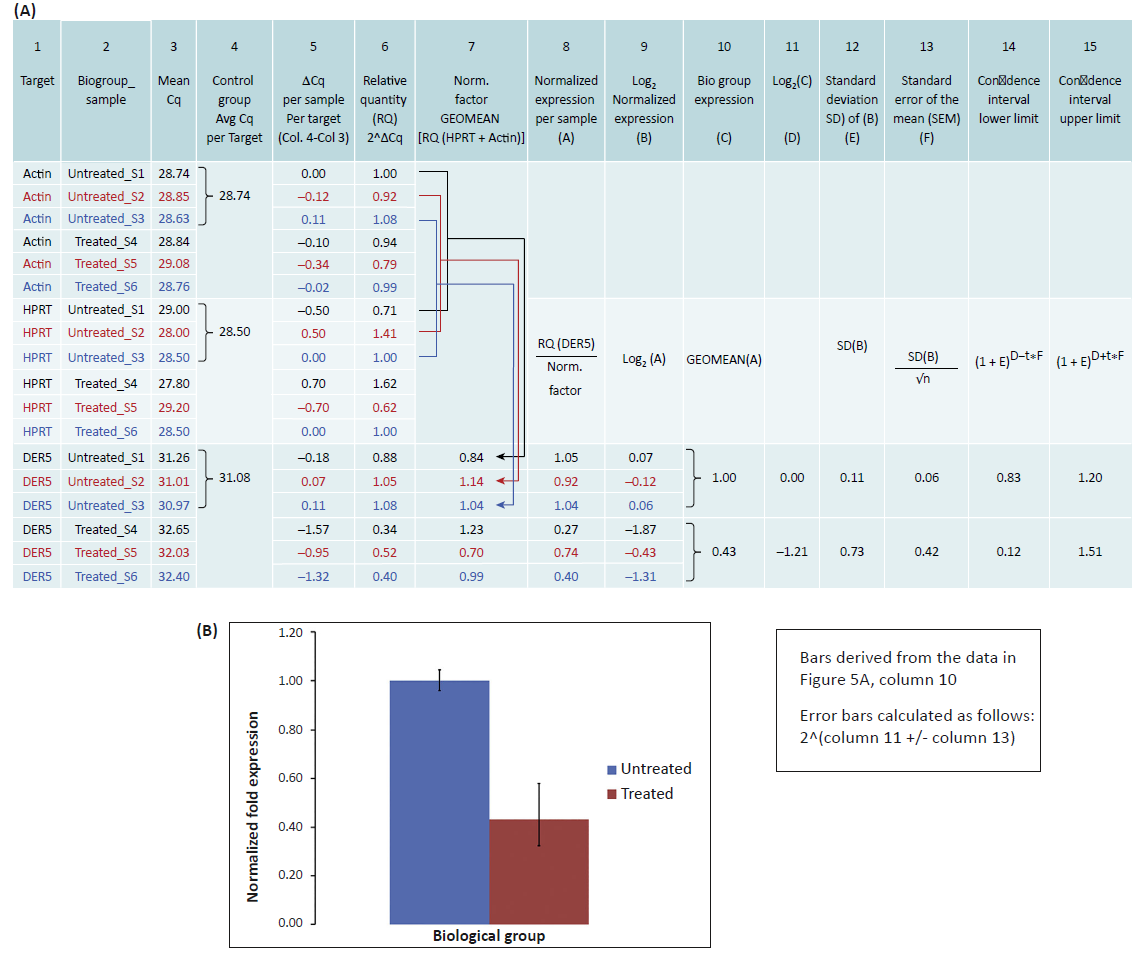
可能的问题及解决方法
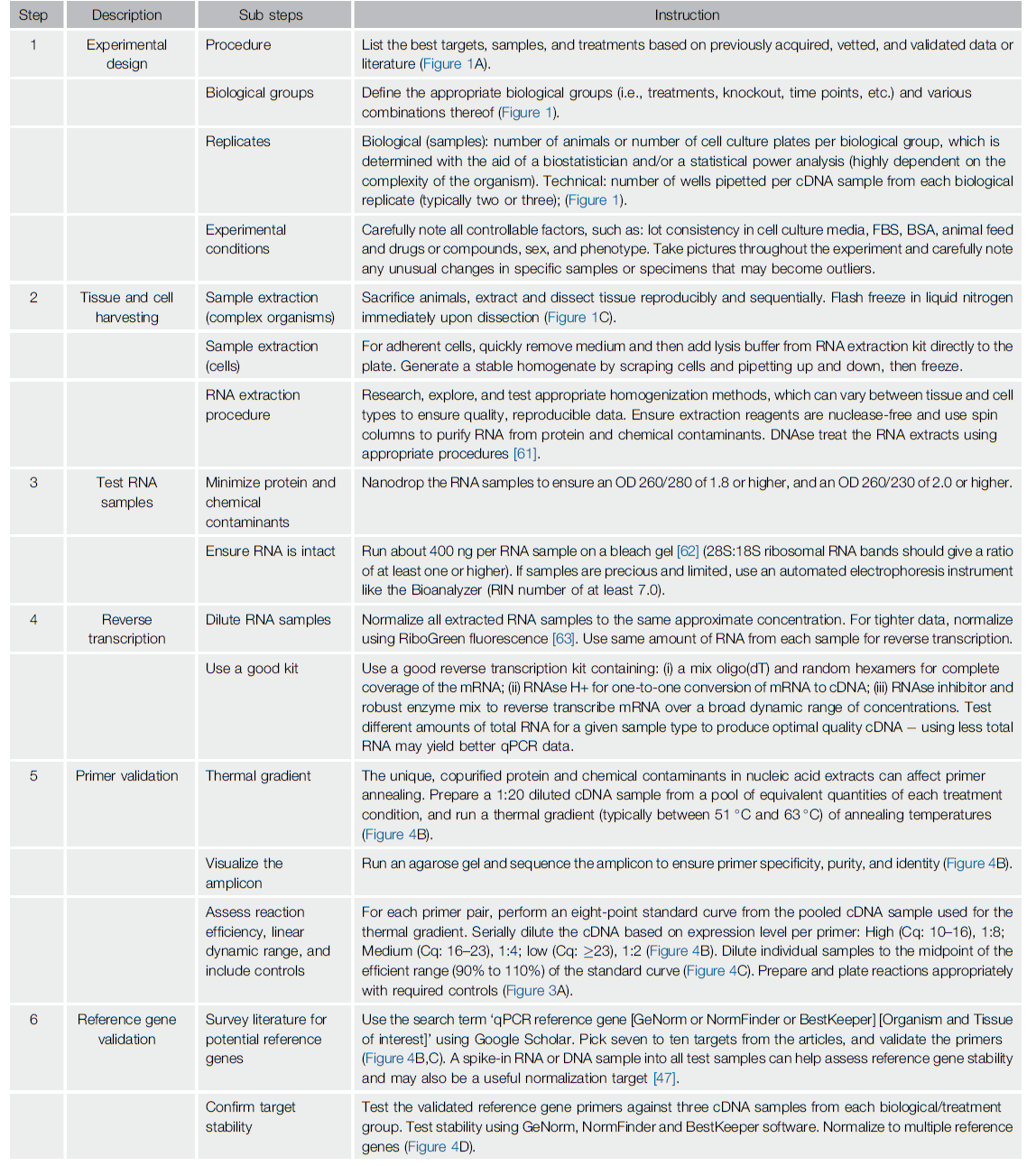
qPCR:从样品采集到表达量计算
https://lixiang117423.github.io/article/qpcrfromsample2expression/